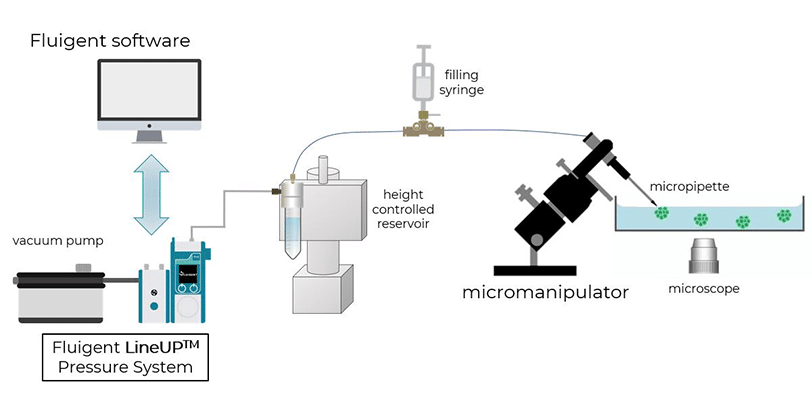
세포 및 조직의 미세 피펫 흡인
미세 피펫 흡인은 단일 세포나 조직의 생체역학적 특성이 세포 형태, 세포의 기계적 자극에 대한 반응, 비종양 상태에서 종양 상태로의 전환 또는 형태 형성 등을 어떻게 조절하는지 평가하기 위한 강력한 비침습적 기술입니다.
Fluigent MFCS™-EZ 및 Flow EZ™ 압력 컨트롤러는 이 방법에 매우 적합합니다. 이 방법에서는 10pN에서 1nN까지 정확히 힘을 가해야 하기 때문입니다.
우리는 세포의 기계적 특성을 어떻게 측정합니까?
세포의 기계적 특성은 무엇입니까?
세포핵의 기계적 특성은 많은 생물학적 과정에서 중요한 요소로 점차 인식되고 있습니다. 핵의 변형 가능성은 면역 세포와 암 세포가 조직과 내피 세포 층을 통과하여 이동할 수 있는 능력을 결정합니다. 핵의 기계적 특성 변화는 또한 암 진행 및 줄기 세포 분화 과정에서 새로운 바이오마커로 사용될 수 있습니다 [5].
현재 사용 중인 기술
그러나 현재 핵의 점탄성 기계적 특성을 측정하는 기술은 시간이 많이 소요되며, 한 번에 하나의 세포만 조사할 수 있거나 고도로 전문화된 장비를 필요로 합니다. 또한, 많은 현재의 검사 방법은 점탄성 물질의 특징인 시간 의존적인 특성을 측정하지 않습니다 [5, 6].
미세 피펫 흡인은 정밀하고 민감한 음압을 적용하여 세포를 미세 피펫을 통해 빨아들이는 원리를 사용합니다. 먼저 세포를 미세 피펫의 끝에 고정한 후, 흡입을 통해 세포를 튜브 안으로 끌어들입니다.
왜 미세 피펫 흡인 기법을 사용합니까?
미세 피펫 튜브를 통과한 세포 부분의 이동 거리를 정량화하기 위해 현미경을 사용해 세포의 위치를 추적할 수 있습니다. 이러한 행동은 세포를 스프링과 댐퍼의 조합으로 모델링하는 집중 매개변수 모델에 의해 예측됩니다(각각 강성과 점성을 나타냄) [5].
미세 피펫 흡인 중 세포가 보이는 변형은 강성 때문에 선형 탄성 반응과 점성 행동 때문에 크립 반응을 보입니다. 이러한 반응은 세포 유형마다 다릅니다. 예를 들어, 백혈구는 연골 세포보다 낮은 강성을 나타냅니다. 이 강성 차이는 세포 간 상호작용 방식과 주변 환경에 영향을 받는 방식에 영향을 미칩니다. 마이크로 피펫 흡인은 다양한 세포 유형에서 강성을 정량화할 수 있는 다목적 기술입니다.
세포의 기계적 특성을 정량화할 수 있다면 다른 병리학적 상태를 조사하고 진단하는 데 유용한 도구가 될 수 있습니다. 섬세한 개별 세포를 처리하고, 이를 조작하는 데 필요한 작은 힘과 그들의 작은 크기를 감안할 때, 재료 속성을 측정하기 위해 전통적인 방법을 사용하는 것은 현실적이지 않습니다.
마이크로 피펫 흡인의 장점
- 비침습적: 미세 피펫 흡인은 동일한 샘플에 대해 반복적인 측정이 가능합니다. 조직 내 개별 세포의 세포 긴장 변화를 시간이 지남에 따라 모니터링할 수 있습니다. 이 방법은 형태 형성을 유도하는 시공간적 긴장 맵을 추적하는 강력한 도구입니다 (Maitre et al, Nat Cell Biol, 2015).
- 경제적이고 사용 및 구축이 쉽다: Fluigent의 미세 피펫 흡인은 컴팩트하며 어떤 현미경에도 맞출 수 있고 직관적인 소프트웨어로 제어됩니다. AFM, 세포 압입기 및 광학 핀셋과 같은 경쟁 기술은 비싸고 특정 교육이 필요하며 전용 현미경이 필요할 수 있습니다.
- 시간 절약: Fluigent 제품의 반응성 덕분에 지정된 압력이 즉시 세포 표면에 적용됩니다(밀리초 범위). 세포 표면 장력은 3~5분 안에 측정할 수 있습니다(Maitre 등, Nat Cell Biol, 2015).
- 운영자 간 변동이 없다: 숙련된 인력이 필요할 뿐만 아니라, 수동 흡인은 적용되는 압력을 정확하게 정량화할 수 없기 때문에 상당한 운영자 간 변동이 발생합니다. 대조적으로, Fluigent 압력 조절기는 항상 0.1%의 정확도로 설정된 압력을 제공합니다.
- 고감도 및 고해상도: Fluigent 기기는 저압(0.1-10mbar)에서 작은 압력 증분(0.007mbar)을 제공하는 유일한 제품입니다. 이들은 공초점 현미경으로는 접근할 수 없는 세포 골격 구조 및 조직 변경과 같은 아세포 역학을 조사할 수 있게 해줍니다.
미세 피펫 흡인 기술의 응용
미세 피펫 흡인은 여전히 핵 역학을 연구하는 데 있어 가장 일반적으로 사용되는 도구 중 하나이며, 다양한 시간 척도에서 핵의 점탄성 행동에 대한 중요한 정보를 제공합니다.
마이크로 피펫 흡인은 핵의 기계적 특성, 염색질에서 핵질 배제, 그리고 염색질 스트레칭 등 다양한 현상을 연구하는 데 사용되었습니다 [5].
이미지는 프랑스 Institut Curie의 Jean-Léon Maitre 제공.
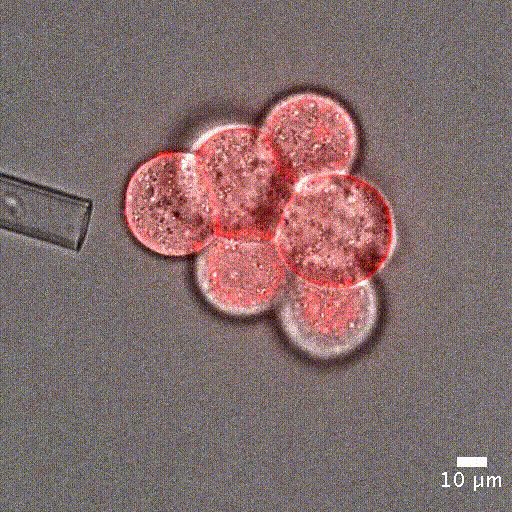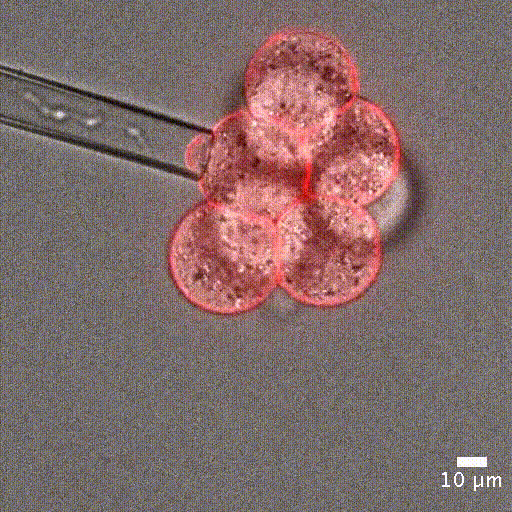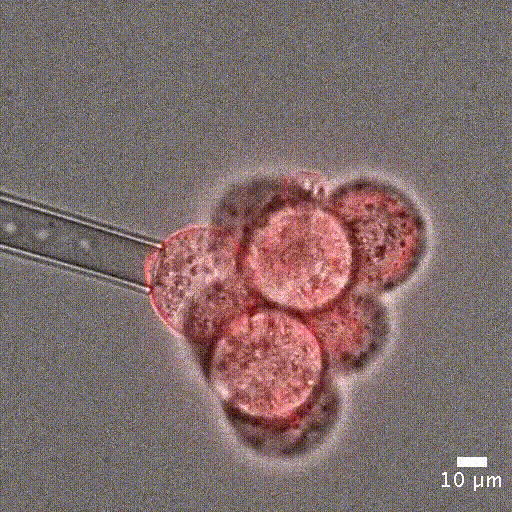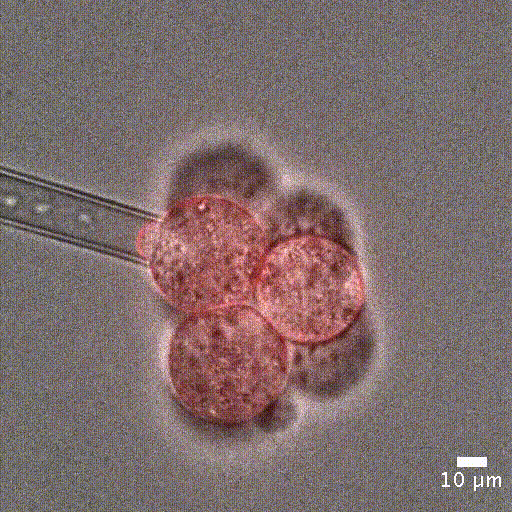
세포 기계적 특성 측정 : 많은 생물학적 과정은 세포 강성의 변화 로 특징지어집니다. 예를 들어, 세포가 유사분열에 진입할 때 [1], 종양 세포가 전암 단계로 전환될 때 [2], 말라리아에 감염된 적혈구 [3] 등이 있습니다. 이러한 기계적 변화는 세포 수준에서 발생하며, 정확한 측정이 필요합니다. 이를 통해 세포 강성을 정밀하게 정량화할 수 있습니다.
듀얼 피펫 흡인 분석법 : 이는 세포 흡인 설정의 복제 버전으로, 접촉 중인 세포들을 분리하여 세포-세포 간 긴장과 세포-매질 간 긴장의 상대적인 기여도를 평가하는 데 유용한 도구입니다 (Maitre et al., Science, 2012).
단일 세포 조작 : 마이크로 피펫 흡인 은 단일 세포 또는 세포 클러스터의 공간적 위치를 조정할 수 있게 해줍니다. 단일 세포 위치 선정은 단일 세포 분석이나 클론 세포주 개발에 필수적입니다.
조직 내 긴장의 불균일성 : 단일 세포 수준에서 세포 긴장을 평가하면 조직의 공간적 긴장 맵을 매핑할 수 있습니다. 이 방법은 특히 조직 형태 형성 또는 배아 발생을 유도하는 힘을 조사하는 데 매우 효과적입니다(Maitre 等,2016,Nature)。
체외 진단 : 현미경으로 확인하거나 감지할 수 없는 비정상적인 행동을 탐지하기 위해 세포 수준에서 강성을 측정하는 것은 강력한 도구입니다. 예를 들어, 수정 후 몇 시간 내에 배아의 생존 가능성을 예측할 수 있습니다. 이 단계에서는 생존 가능한 배아와 그렇지 않은 배아를 형태학적으로 구별할 수 없지만, 기계적 특성 을 통해 이를 구분할 수 있습니다 [4].
마이크로 피펫 흡인 패키지

마이크로fluidic 유량 컨트롤러

마이크로fluidic 소프트웨어 제어
실시간 제어 및 실험 자동화 소프트웨어

디지털 고속 현미경

마이크로 피펫 흡인 패키지
자세한 정보 또는 기술 상담
참조
[1] Théry M, Bornens M, Get round and stiff. 2008, HFSP J, 2(2):65-71.
[2] Tavares S et al, actin stress fiber organization promotes cell stiffening and proliferation of pre-invasive breast cancer cells. 2017, Nat Commun. 8:15237.
[3] Guo Q et al, Microfluidic biomechanical assay for red blood cells parasitized by Plasmodium falciparum. 2012, Lab Chip; 12(6):1143-50.
[4] Yanez LZ et al, human oocyte developmental potential is predicted by mechanical properties within hours after fertilization, 2016, Nat Commun. 7:10809
[5] Davidson, P.M. et al. (2019) “High-throughput microfluidic micropipette aspiration device to probe time-scale dependent nuclear mechanics in intact cells,” Lab on a Chip, 19(21), pp. 3652–3663. Available at: https://doi.org/10.1039/c9lc00444k.
[6] González-Bermúdez, B., Guinea, G.V. and Plaza, G.R. (2019) “Advances in micropipette aspiration: Applications in cell biomechanics, models, and extended studies,” Biophysical Journal, 116(4), pp. 587–594. Available at: https://doi.org/10.1016/j.bpj.2019.01.004.
고객이 엄선한 출판물
Guevorkian K,Maître JL.Micropipette aspiration: A unique tool for exploring cell and tissue mechanics in vivo.MethodsCellBiol. 2017;139:187-201
Maître JL et al, Asymmetric division of contractile domains couples cellpositioning and fate specification, Nature. 2016 Aug 18;536(7616):344-34
Biro M, Maître JL, Dual pipette aspiration: a unique tool for studying intercellular adhesion.MethodsCellBiol. 2015;125:255-67
Porazinski S et al, YAP is essential for tissue tension to ensure vertebrate 3D body shape.Nature. 2015 May 14;521(7551):217-221
Maître JL et al, Pulsatile cell-autonomouscontractility drives compaction in the mouse embryo. Nat Cel lBiol. 2015 Jul;17(7):849-55
Maître JL et al, Adhesion functions in cell sorting by mechanically coupling the cortices of adhering cells.Science. 2012;338(6104):253-6