Mikrofluidik für Organ-on-Chip-Anwendungen
Was sind Organ-on-Chip?
Bei der Organ-on-Chip (OOC)-Technologie (Abbildung 1) werden Funktionen oder Krankheiten auf der Ebene menschlicher Organe mit Hilfe von Zellen (in 2D oder 3D) oder Gewebeschnitten in einem mikrofluidischen Chip nachgebildet. Die Mikrofluidik ermöglicht eine präzise Kontrolle der zellulären Umgebung und bietet den Zellen genauere mechanische und biochemische Hinweise (1). Durch die Manipulation kleiner Flüssigkeitsvolumina können diese Modelle skalierbare, dynamische Zellinteraktionen ermöglichen. Die Kombination von Mikrofluidik und OOC-Technologie ermöglicht die Nachbildung menschlicher Organfunktionen zur Untersuchung der menschlichen Physiologie und Krankheit.
Jüngste Fortschritte bei mikrofluidischen Chipdesigns nutzen Geometrien und Strukturen, um physiologische Bedingungen wie Längenskalen, Konzentrationsgradienten und flüssigkeitsinduzierte mechanische Kräfte zu simulieren. Diese biomimetischen Plattformen überwinden viele Einschränkungen, mit denen herkömmliche Gewebekulturmodelle konfrontiert sind.
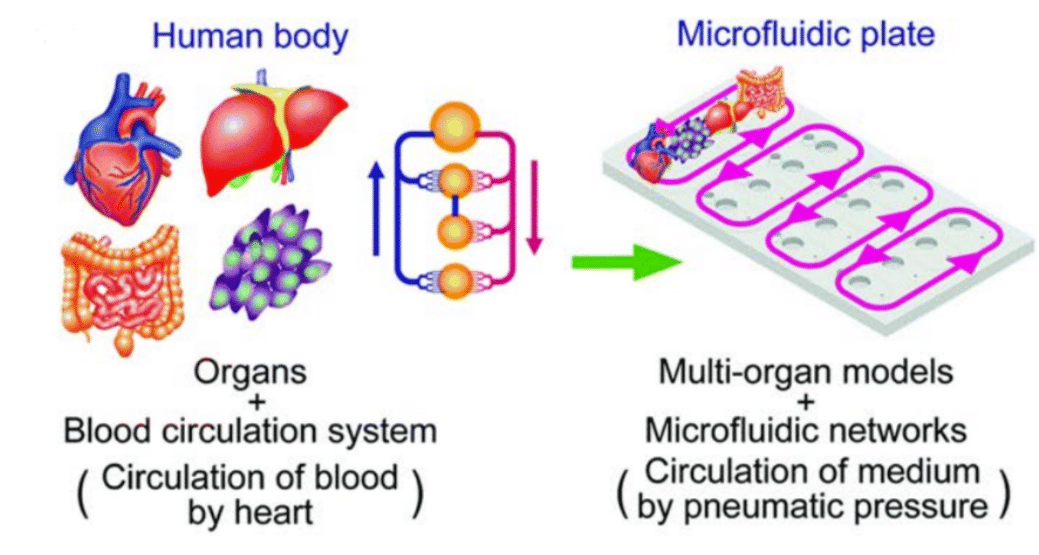
Abbildung 1: Von lebenden Organen zu Organen auf dem Chip .
Anwendungen der Organ-on-chip-Technologie
Entwicklung von Therapien
Organ-on-Chip-Modelle bieten eine bemerkenswerte Vielseitigkeit für das Screening und die Entwicklung von Medikamenten durch innovative technische Methoden und Materialien.
Ein bedeutender Trend zeichnet sich in der Forschung ab, bei der humane induzierte pluripotente Stammzellen (hiPSC) zur Schaffung personalisierter Organmodelle eingesetzt werden. Diese Modelle erleichtern die Erforschung komplexer Kulturaufbauten, indem sie ein Kulturgefäß mit einem mikrofluidischen Kanal unter Verwendung einer porösen Membran verbinden. Diese Konfiguration ist ein ideales Werkzeug für die Untersuchung von Luft-Flüssigkeits-Grenzflächen-Kulturen (ALI), Endothel-/Epithelbarrieren und interzellulärer Kommunikation.
Entdeckung von Arzneimitteln
Die Weiterentwicklung von In-vitro-Organ-on-Chip-Modellen ist vielversprechend für die Vorhersage menschlicher Reaktionen auf neue Arzneimittel. Diese OOC-Modelle bereiten den Weg für präzise Prognosen und detaillierte Untersuchungen der durch potenzielle Arzneimittel verursachten Vergiftungen beim Menschen. Darüber hinaus erleichtern sie die Erforschung neuer therapeutischer Strategien zur Bekämpfung der beobachteten toxischen Wirkungen. Im Rahmen der Arzneimittelforschung ermöglichen die Erkenntnisse aus diesen Modellen die frühzeitige Identifizierung, Modifizierung und Optimierung von Leitwirkstoffen und fördern so die Entwicklung sichererer Arzneimittel mit höheren Erfolgsaussichten in klinischen Studien.
Personalisierte Medizin
Organ-on-Chip-Modelle sind unschätzbare Ressourcen für die präzise Vorhersage und Untersuchung potenzieller arzneimittelbezogener Toxizitäten beim Menschen. Sie ermöglichen eine umfassende Analyse der Auswirkungen verschiedener Chemikalien auf patientenspezifisches menschliches Gewebe. Darüber hinaus ebnen sie den Weg für die Erforschung neuer therapeutischer Möglichkeiten, um den beobachteten schädlichen Wirkungen dieser Substanzen entgegenzuwirken. Im Rahmen der Arzneimittelentdeckung helfen die aus diesen Modellen gewonnenen Erkenntnisse nicht nur bei der frühzeitigen Identifizierung, sondern ermöglichen auch die Modifizierung und Optimierung von Leitsubstanzen. Letztlich fördert dieser Forschungsansatz die Entwicklung von sichereren Medikamenten und erhöht deren Erfolgsaussichten in strengen klinischen Studien.
Präzises Fluidhandeling für Organ-on-chip-Anwendungen
Präzises Fluidhandeling ist ein entscheidender Aspekt von Organ-on-Chip-Anwendungen, da es die genaue Simulation physiologischer Bedingungen gewährleistet und verschiedene Konstellationen ermöglicht. Um ein präzises Fluidhandling bei OOC-Anwendungen zu erreichen, werden mikrofluidische Komponenten wie Mikropumpen, Ventile und mikrofluidische Kanäle eingesetzt. Diese Systeme ermöglichen es den Forschern, Durchflussraten, Gradienten und dynamische Veränderungen der Flussszusammensetzung zu steuern und so eine physiologisch relevante Umgebung für die Untersuchung von Organen und Geweben auf einem Chip zu schaffen.
Warum ist das präzise Fluidhandeling in OOC-Modellen so wichtig?
Nachahmung physiologischer Bedingungen
Organ-on-Chip-Geräte erfordern eine präzise Steuerung der Flussströmung, um die dynamische Mikroumgebung menschlicher Organe genau nachzubilden. Diese Kontrolle stellt sicher, dass die Zellen ähnlichen Scherspannungen und Gradienten ausgesetzt sind, wie im menschlichen Körper.
Studien zu zellulären Wechselwirkungen und Tissue Engineering
Die genaue Handhabung von Fluiden ermöglicht die Untersuchung zellulärer Interaktionen, wie zum Beispiel der Interaktionen zwischen Endothel und Epithel oder der Blut-Hirn-Schranke, die für das Verständnis von Krankheiten und Arzneimittelreaktionen von wesentlicher Bedeutung sind. Sie ist auch entscheidend für die Schaffung von Nährstoffgradienten oder Signalmolekülen innerhalb des Chips, die das Gewebewachstum und die Reifung in künstlich hergestellten Geweben fördern.
Arzneimitteltests und -entwicklung
Das richtige Fluidhandeling erleichtert die Verabreichung von Medikamenten oder Verbindungen in bestimmten Konzentrationen und Raten und ermöglicht so präzise Medikamententests und Screenings auf Wirksamkeit und Schädlichkeit.
Automatisierung und Hochdurchsatzverfahren
Präzise Fluid-Handling-Systeme können automatisiert werden und ermöglichen Experimente und Screening von Substanzen oder Bedingungen im Hochdurchsatzverfahren.
Beispiele für OOC-Modelle
Lung-on-chip – Das erste OoC
Die innovative menschliche Lungenalveole auf einem Chip (Abbildung 2) definiert die Organ-on-Chip (OoC)-Technologie neu, indem sie integrierte physiologische und pathophysiologische Reaktionen nachbildet und damit frühere Modelle übertrifft, die sich hauptsächlich auf Zell- oder Gewebefunktionen konzentrierten. Dieses bahnbrechende Organmodell besteht aus zwei parallelen Mikrokanälen, von denen einer mit menschlichen Lungenepithelzellen und der andere mit menschlichen Endothelzellen ausgekleidet ist, die durch eine mikroporöse Membran voneinander getrennt sind.
Nach Erreichen der Zellkonfluenz entsteht durch die Einführung von Luft in das Epithelkompartiment eine Luft-Flüssigkeits-Grenzfläche, die die Auskleidung des alveolären Luftraums nachahmt. Dieses kompartimentierte Mikrogerätedesign ermöglicht eine präzise Steuerung des Flusses, der Zellzufuhr und der Nährstoffverteilung unabhängig von Epithel und Endothel.
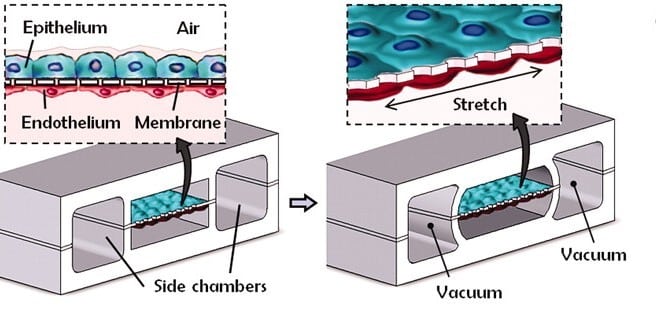
Abbildung 2: Biologisch inspiriertes Design einer atmenden menschlichen Lunge auf einem Mikrochip (2).
Darm-auf-Chip
Sowohl für den Dünn- als auch für den Dickdarm wurden mehrere innovative Modelle der Organ-on-Chip (OoC)-Technologie entwickelt, bei denen Darmepithelzellen mit oder ohne darunter liegendes Endothel verwendet werden. Diese Modelle dienen einem doppelten Zweck: der Nachbildung verschiedener Krankheiten und der Untersuchung des Arzneimittelstoffwechsels und der Toxizität.
Im Dünndarm-Chip wurde die dynamische Flüssigkeitsströmung als Schlüsselfaktor identifiziert, der die Zottenbildung und die Produktion von Becherzellen fördert, während er gleichzeitig den Aufbau einer schützenden Schleimschicht in Dickdarm-Chips begünstigt. Darüber hinaus ist die Nachahmung von peristaltikähnlichen mechanischen Bewegungen für eine optimale Gewebedifferenzierung entscheidend. So förderten zyklische mechanische Dehnungen und die Verbesserung des Flüssigkeitsflusses in Colon-on-Chip-Modellen das Wachstum von Bakterien, zum Beispiel von Shigella-Bakterien.
Tumor-auf-Chip
Tumor-on-Chip-Modelle entwickeln sich rasch zu leistungsfähigen Instrumenten in der Onkologieforschung. Diese innovativen Systeme bilden entscheidende Elemente der Tumormikroumgebung (TME) wirksam nach, darunter biochemische Gradienten, Nischenfaktoren, komplizierte Zellinteraktionen und komplexe Gewebestrukturen aus Tumor- und Stromazellen (3). Tumor-on-Chip-Designs zielen auf die Nachbildung von Gewebe-Gewebe-Schnittstellen ab und sind von zentraler Bedeutung für die Nachbildung der komplexen Interaktionen während der Krebsinvasion und Metastasierung. Zahlreiche Modelle wurden entwickelt, um die Tumor-Umgebung zu untersuchen und das Verhalten von Tumorzellen zu erforschen. Zum Beispiel die Reaktion von Zellen auf Stoffwechselgradienten. Ein weiteres Beispiel ist der Einsatz von TOC-Modellen, die das Verständnis des Stoffwechsels und der Arzneimittelresistenz von Tumorzellen in einer hypoxischen Umgebung in vivo erleichtern. Diese innovative Plattform ist vielversprechend, um entscheidende Aspekte des Tumorverhaltens zu entschlüsseln und Strategien zur Bewältigung der damit verbundenen Herausforderungen zu entwickeln.
Fluigents Beitrag zum OOC-Bereich
Bei Fluigent dreht sich alles um die Förderung des wissenschaftlichen Fortschritts, insbesondere auf dem dynamischen Gebiet der Organ-on-Chip-Technologie. An vorderster Front suchen wir ständig nach neuen Wegen, um die Forschung voranzutreiben, und streben danach, innovative Lösungen zu entwickeln, die die Grenzen der wissenschaftlichen Erforschung neu definieren.
Unser Ziel ist es, neue Entwicklungen voranzutreiben, die die Organ-on-chip-Landschaft revolutionieren. Wir haben uns der Beschaffung und Bereitstellung innovativer Lösungen verschrieben, die es Forschern ermöglichen, biologische Systeme mit größerer Präzision und Effizienz zu erforschen.
Referenzen
- Wu, Q.; Liu, J.; Wang, X.; Feng, L.; Wu, J.; Zhu, X.; Wen, W.; Gong, X. Organ-on-a-chip: Recent breakthroughs and prospects. Biomed. Eng. Online 2020, 19, 9.
- Huh, D. et al. Reconstituting Organ-Level Lung Functions on a Chip. Science (1979) 328, 1662– 1668 (2010).
- Imparato, G., Urciuolo, F. & Netti, P. A. Organ on Chip Technology to Model Cancer Growth and Metastasis. Bioengineering 9, 28 (2022)